Enfermedad por Listeria monocytogenes. Minireview: Listeriosis invasiva en adultos
Enfermedad por Listeria monocytogenes.
Minireview: Listeriosis invasiva en adultos.
Dra. Daniela Paciel, Dr. PhD. Julio Medina.
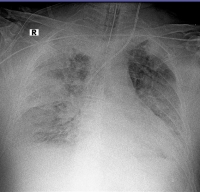
«La listeriosis, enfermedad causada por Listeria monocytogenes, es fundamentalmente una enfermedad transmitida por alimentos, de notificación obligatoria, que puede ser de difícil diagnóstico, pudiendo presentarse como cuadros clínicos graves.[1,2] Luego de la salmonelosis es la segunda causa más frecuente de muertes relacionadas con infecciones transmitidas por alimentos en Europa y EE.UU.[3]»
Management of infections in critically ill returning travellers in the intensive care unit—II: clinical syndromes and special considerations in immunocompromised patients
Management of infections in critically ill returning travellers in the intensive care unit—II: clinical syndromes and special considerations in immunocompromised patients
Comentario:
Dra. Daniela PacielLos autores de este Consenso resaltan los siguientes aspectos:
- Los pacientes con diferentes grados de inmunodepresión (como los receptores de trasplante de órgano sólido) puede viajar a diferentes países incluso a países con recursos limitados en el post-trasplante a lo largo de los años.
- En los últimos años emergen las fiebres hemorrágicas graves que pueden tener como principal manifestación en los paísas desarrollados un síndrome de fuga capilar cuando el remplazo de volumen es adecuado, a diferencia de los países de bajos recursos.
- Los viajeros que se presentan a su regreso con síndrome respiratorio agudo tienen en general una neumonía.
- Se presenta el consenso de la ESCMID sobre el manejo de viajeros que retornan y se presentan como pacientes críticos, destinada a intensivistas, especialistas en enfermedades infecciosas y médicos de emergencia con un enfoque estandarizado para el tratamiento de infecciones graves en este contexto.
- Se compone de diferentes secciones en las que se considera que la globalización actual por viajes interconentales a zonas endémicas así como las migraciones debidas a conflictos armados han cambiado las etiologías planteables. Por otra parte, la población de pacientes inmunodeprimdos se encuentra en aumento (TOS, TMO, pacientes con biológicos, etc).
- Sin ser exhaustivo, este consenso presenta el riesgo de diferentes poblaciones frente a la tuberculsois, dengue, malaria, fiebres hemorrágicas, etc. y da linemientos para el diagnóstico y manejo de las diferentes etiologías posibles.
Hepatopatía y VIH
Hepatopatía y VIH
- La peritonitis bacteriana espontánea
- TARV en hepatopatía
- Trasplante hepático en Pacientes con VIH
Residente Dra. Elisa Cabeza
Prof. Adj. Dra. G. Pérez Sartori
Agosto de 2016
Guías Consolidadas de Terapia Antirretroviral de la Organización Mundial de la Salud
En junio de 2016 fue publicada una nueva edición de las Guías Consolidadas de Terapia Antirretroviral de la Organización Mundial de la Salud [1] Las recomendaciones se diferencian según el tipo de epidemia: generalizada (mayor a 1% en población general) o concentrada (prevalencia menor a 1% en población general que coexiste con grupos mas vulnerables con prevalencia mayor a 5%).
Estas guías se enfocan en el uso de antirretrovirales como tratamiento y como prevención en todo el continuo de atención de pacientes con VIH y con una aproximación de salud pública: intervenciones sencillas incluyendo esquemas de tratamiento antirretroviral (TARV) en co-formulaciones que permitan un abordaje simplificado y faciliten la ampliación del acceso.
Como recomendaciones a considerar en nuestro contexto se destacan:
- Utilizar estrategias de diagnóstico sencillas (algoritmos simplificados) asegurando la calidad de las pruebas, la capacitación del personal en el uso de pruebas rápidas, y siempre confirmar con una segunda prueba una primera reactiva, antes de iniciar el TARV
- Inicio inmediato de TARV en niños/as con el primer test virológico positivo y extraer la muestra para un segundo estudio
- Además de las poblaciones clave priorizar otras poblaciones en el acceso al testeo facilitado como: adolescentes, las parejas de personas con diagnóstico de VIH y las parejas de mujeres embarazadas
- Implementar estrategias de prevención combinada que incluyan profilaxis pre exposición en personas en riesgo “sustancial”
- Iniciar TARV en todo paciente en que se realiza el diagnóstico de VIH independientemente de CD4 y estadio clínico
- Iniciar TARV en todo/a niño/a en que se realiza el diagnóstico de VIH independientemente de CD4 y estadio clínico
- En adultos, adolescentes, mujeres embarazadas se mantiene como recomendación de plan de inicio: TDF + 3TC (o FTC) + EFV pero como uno de los planes alternativos se incluye TDF + 3TC (o FTC) + DGV
- El monitoreo con carga viral luego cuando el paciente se encuentra bajo TARV estable y con buena respuesta (carga viral suprimida) puede realizarse cada 6 meses
También se incorporan recomendaciones respecto a uso de cotrimoxazol como profilaxis, tratamiento de la infección tuberculosa latente, técnicas diagnósticas de tuberculosis, así como terapia anticipada para criptococosis en determinadas situaciones.
Gripe grave en paciente inmunodeprimido
Gripe grave en paciente inmunodeprimido
Dra. Cecilia Villarino
Prof. Adj. Daniela Paciel
17 de junio 2016
Multiresistencia en Uruguay: lugar de la fosfomicina intravenosa y vía oral
Gripe: diagnóstico de severidad, uso de antivirales y medidas generales
Vacunación contra la gripe en el año 2016: los virus circulantes son concordantes con las cepas incluidas en la vacuna trivalente en el 91% de los casos
-
Vacunación contra la gripe en el año 2016
(
 Descargas)
Descargas)